题型:实验探究题 题类:模拟题 难易度:普通
湖北省宜昌市2017-2018学年高考理综-化学4月模拟考试试卷
猜想 2: (写出化学方程式)。
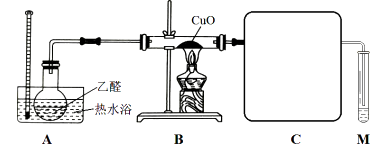
已知: 乙醛和乙酸的沸点分别为 20.8℃、 117.9℃。
按上述装置进行实验,当氧化铜完全反应后停止实验。
①为达到良好的冷凝效果,方框中 C 装置应选用(填仪器名称);实验中先通入乙醛蒸气,后点燃装置 B 处酒精灯,这样操作的目的是。
②已知: Cu2O 呈红色,在酸性条件下发生反应 Cu2O+2H+=Cu+Cu2++H2O。 请你设计实验证明猜想 1 成立。
实验操作: 。
实验现象: 。

已知:醋酸亚铬[Cr(CH3COO)2]溶液可以吸收少量的 O2。
①下列有关说法正确的是(填标号) 。
a. 装置 D 可以控制反应的发生与停止
b. 装置 F 中盛装醋酸亚铬溶液
c. 向装置 D 中加入少量硫酸铜固体可加快反应
d. 实验中观察到装置 G 中有明显现象
②装置 G 中红色粉末完全反应后,称得固体粉末质量为 19.2 g;装置 H 净增质量为2.0 g。请选择合理数据计算,确定红色粉末的成分及物质的量: 。
选项 | 实验操作 | 发生的现象 | 解释或结论 |
A | 向亚硫酸钠溶液中,逐滴加入硝酸酸化的硝酸钡溶液 | 产生白色沉淀 | 产生的亚硫酸钡是难溶解入水的沉淀 |
B | 将SO2通入滴有酸性高锰酸钾溶液中 | 溶液紫红色褪去 | SO2具有漂白性 |
C | 常温下铜片插入硝酸中 | 产生红棕色气体 | 常温下铜硝酸一定产生NO2 |
D | 向某溶液中加入NaHCO3 | 产生白色沉淀 | 该溶液可能原来含有氢氧化钡 |
| 选项 | 实验内容 | 实验目的 |
| A | 室温下,用pH试纸分别测定浓度均为0.1mol·L-1的的NaClO溶液和CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| B | 向AgCl悬浊液中滴入0.1mol·L-1的的NaI溶液,悬浊液变黄 | 证明相同温度下:Ksp(AgCl)>Ksp(AgI) |
| C | 常温下,测得饱和溶液的pH: NaA>NaB | 证明常温下的水解程度:A-<B- |
| D | 酸式滴定管中硫酸液面在20.00mL处,将滴定管中液体全部放出 | 量取20.00mL硫酸溶液 |
| 选项 | 实验目的 | 实验操作 |
| A | 探究浓度对反应速率的影响 | 向2支各盛有4mL0.01mol·L-1KMnO4酸性溶液的试管中,分别加入2mL0.1mol·L-1H2C2O4溶液和2mL0.2mol·L-1H2C2O4溶液,记录溶液褪色所需的时间 |
| B | 配制1.00mol·L-1的NaOH溶液 | 称取4.0g固体NaOH于烧杯中,加入少量蒸馏水溶解,然后转移至100mL容量瓶中定容 |
| C | 探究固体表面积对反应速率的影响 | 称取相同质量的大理石和纯碱,加入到盛有浓度、体积均相同的盐酸的小烧杯中,观察实验现象 |
| D | 探究淀粉溶液在稀硫酸和加热条件下是否水解 | 取少量的水解液于试管中,先加适量的NaOH溶液,再滴入碘水,观察实验现象 |
试题篮