题型:综合题 题类:模拟题 难易度:普通
陕西省榆林市2018-2019学年高考理综-化学模考试卷
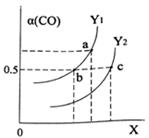
如图表示CO的平衡转化率(α)随温度和压强变化的示意图。X表示的是,Y1Y2(填“<”、“=”、“>”)。

①反应进行到4min时,v(正)v(逆)(填“>”“<”或“=”)。0~4min,CO2的平均反应速率v(CO2)=mol·L−1·min−1。
②该温度下平衡常数为。
③下列能说明该反应已达到平衡状态的是。
A.v正(CH3OH)=3v逆(H2)
B.CO2、H2、CH3OH和H2O浓度之比为1∶3∶1∶1
C.恒温恒压下,气体的体积不再变化
D.恒温恒容下,气体的密度不再变化
试题篮