题型:单选题 题类:常考题 难易度:普通
黑龙江省哈尔滨市第六中学2020-2021学年高一上学期化学12月月考试卷
实验序号 | 实验现象 | 实验结论 |
A | 氯水呈浅绿色 | 氯水中含有含有Cl2 |
B | 向FeCl2溶液中滴加氯水,溶液变成棕黄色 | 氯水中含有HClO |
C | 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀 | 氯水中含有Cl﹣ |
D | 向氯水中加入NaHCO3粉末,有气泡产生 | 氯水中含有H+ |
在实验室里可用如图1所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.

图1中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里盛有紫色石蕊溶液.
请回答下列问题:
(1)仪器a的名称是{#blank#}1{#/blank#} .
(2)实验室制取氯气的离子方程式为{#blank#}2{#/blank#} .为了除去氯气中的氯化氢气体,可在①与②之间安装盛有{#blank#}3{#/blank#} (填字母代号)的净化装置.
A.碱石灰B.饱和食盐水C.浓硫酸D.饱和碳酸氢钠溶液
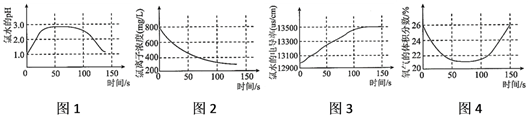
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是{#blank#}4{#/blank#} .反应完毕经冷却后,②的试管中有大量晶体析出.在图2中符合该晶体溶解度曲线的是{#blank#}5{#/blank#} (填字母代号);从②的试管中分离出晶体的操作是{#blank#}6{#/blank#} ,该操作需要用到的玻璃仪器有{#blank#}7{#/blank#} .
(4)次氯酸钠中存在的化学键类型为{#blank#}8{#/blank#} .
(5)实验中可观察到④的试管里溶液的颜色发生了如下变化,请完成下表中的空白:
实验现象 | 原因 |
溶液最初从紫色逐渐变为{#blank#}9{#/blank#} 色 | 氯气与水反应生成的H+使石蕊变色 |
随后溶液逐渐变为无色 | {#blank#}10{#/blank#} |
然后溶液从无色逐渐变为{#blank#}11{#/blank#} 色 | {#blank#}12{#/blank#} |
(6)装置⑤的作用是{#blank#}13{#/blank#} .
试题篮