修改时间:2024-12-16 浏览次数:4 类型:期末考试



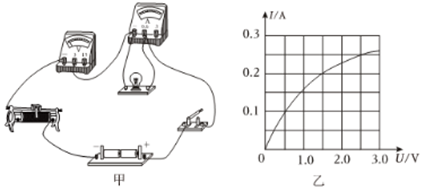
步骤1:利用图甲所示装置,将干燥的氧气从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满氧气后,在导管b处连接一活塞推至底部的注射器,收集20mL氧气后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形管内的铁丝,其现象如下表所示:
观察对象 | ①干燥的普通铁丝 | ②潮湿的普通铁丝 | ③潮湿的纯铁丝 |
现象 | 没有明显变化 | 较多红褐色锈斑 | 没有明显变化 |
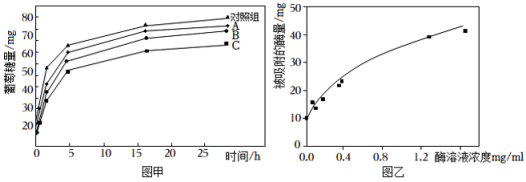
实验一:在等量的纤维素中加入不同种类的木质素A、B、C,再加入等量的酶进行催化分解,多次实验后测得葡萄糖量与时间的关系如图甲。
实验二:分别在各种不同浓度的酶溶液中加入等量的某种木质素,多次实验后得到被吸附的酶的量与酶溶液浓度之间的关系如图乙。
试题篮