修改时间:2022-02-22 浏览次数:115 类型:一轮复习
①取少量固体粉末于试管中,加足量的水溶解,静置后得到白色沉淀A和无色溶液B;
②过滤,将白色沉淀A放入试管中,滴加过量的稀硝酸,有气泡产生,沉淀部分溶解;
③取无色溶液B少许于试管中,滴加过量的稀硝酸,有气泡产生,得到溶液C;
④在溶液C中滴加硝酸银溶液,有白色沉淀产生。
以下说法正确的是( )
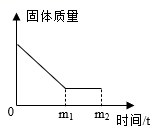
(提出问题)烧杯中溶液的溶质成分是什么?
张南同学猜想溶质成分是:NaNO3、NaCl、HCl
小岗同学猜想溶质成分是:NaNO3、NaCl、Na2CO3
你的猜想是;
张南猜想的理由是。
张南同学为了验证自己的猜想取少量滤液于试管中,向其中滴加少量硝酸银溶液观察到有白色沉淀的实验现象,于是得出结论:自己的猜想正确。请对张南同学由实验得出的的结论进行评价;
通过上述张南、小岗两位同学对溶液溶质成分的猜想,总结出猜想所得溶液中溶质成分时除需考虑可溶性的生成物和可溶性的反应物外,还需考虑的物质。
[查阅资料]
20℃时,部分物质的溶解度。
| 物质 | Ca(OH)2 | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 0.16 | 109 | 21.8 | 9.6 |
20℃时,在盛有5g Ca(OH)2固体的A烧杯中加入40mL水,用玻璃棒搅拌,静置,取上层部分清液于B烧杯中。
①向A烧杯中滴加几滴酚酞溶液,观察到的现象是,再加入过量稀盐酸,反应的化学方程式为
②向B烧杯中通入CO2 , 观察到澄清石灰水变浑浊。
③由上述实验可知氢氧化钙的性质。
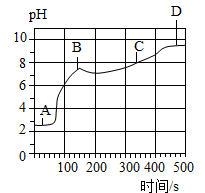
向上述(1)反应后的A烧杯中滴加碳酸钠溶液,测得其pH随反应时间的变化如图。AB段的实验现象是,BC段发生反应的化学方程式为
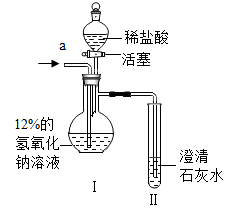
[设计和实验] 20℃时,甲、乙两组同学设计如图装置分别进行实验。
甲组:从a端缓慢通入CO2 , 一段时间后II中变浑浊,停止通CO2 , I中溶质为X。打开活塞,滴加足量稀盐酸。
[解释与结论]
经分析X是NaHCO3。实验过程中,Ⅰ中产生的现象是
[解释与结论]
乙组同学认为Y只有Na2CO3。你认为该结论是否合理,结合分析Y的成分说明理由。I 中一定发生反应的化学方程式为。
试题篮