修改时间:2021-07-23 浏览次数:169 类型:同步测试


| 选项 | 实验室中的废液或废物 | 溶质a |
| A | 剩余的表面已经被氧化的铝片 | H2SO4 |
| B | 氢氧化铜和过量稀盐酸反应后的溶液 | NaOH |
| C | 稀硫酸与过量氢氧化钠溶液反应后的溶液 | BaCl2 |
| D | 碳酸钠溶液和氢氧化钙溶液恰好完全反应后的混合物 | HCl |
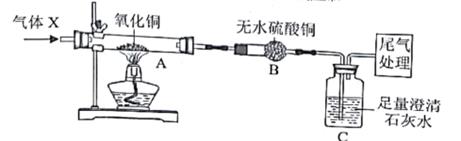
②铜和氧化亚铜均为不溶于水的红色固体;③Cu2O+H2SO4=CuSO4+Cu+H2O
小乐为了探究反应所得红色固体的成分,进行了如下实验: .
|
实验操作 |
|||
|
步骤一 |
取20g红色固体于烧杯中,加入足量稀硫酸 |
|
红色固体可能是氧化亚铜,也可能是铜和氧化亚铜 |
|
步骤二 |
将步骤一反应所得的混合物经过滤、洗涤、干燥并称量剩余红色固体质量 |
剩余红色固体质量为12g |
20g红色固体中,铜和氧化亚铜的质量比为 |

| 装置 | 反应前 | 反应后 |
| A | 试管的质量36.2 克 氧化铜和炭粉混合物的质量20.0克 |
试管和固体物质的质量54.8 克 |
| B | 反应后瓶内液体比反应前增重1.1 克 | |
分析数据发现,反应中消耗碳和氧元素的质量大于生成二氧化碳的质量.下列4项中跟这一结果有关的有哪几项? (填编号)
【提出问题】该滴瓶中溶质的成分是什么?
猜想Ⅰ溶质成分只有:KCl; 猜想Ⅱ溶质成分为:KCl和KOH;
猜想Ⅲ溶质成分为:KCl、K2SO4; 猜想Ⅳ溶质成分为:KCl、KOH和K2SO4 .
【实验探究】为证明猜想,小军设计了如下实验方案,请你一起完成下列实验报告;
|
实验操作 |
实验现象 |
结论或解释 |
|
(1)取该滴瓶内溶液于试管中,向试管中加入适量BaCl2溶液 |
|
溶质中有K2SO4 |
|
(2)将上述反应后的混合液过滤,取滤液于另一支试管中,向该试管中加入酚酞试液 |
|
证明猜想Ⅳ成立 |
试题篮