题型:综合题 题类:模拟题 难易度:普通
广西防城港市2017-2018学年高三理综-化学1月模拟考试试卷
a.含氧酸的酸性:HNO3>H3PO4>H3AsO4
b.原子半径:S >P>As
c.氢化物的稳定性NH3>PH3> AsH3
d.AsH3电子式是 ![]()
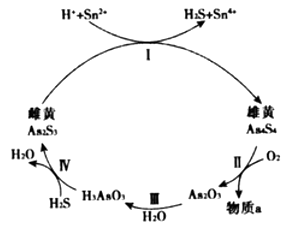
①Ⅱ中若1molAs4S4反应转移28mole- , a物质是。
②Ⅰ中反应的离子方程式是。

①人体血液的pH在7.35~7.45 之间,用药后人体中含砷元素的主要微粒是。
②H3AsO3的一级电离常数是6×10-10mol·L-1 , n(H3AsO3)∶n(H2AsO3-)=1∶1时,溶液的pH=(列出计算式即可)。
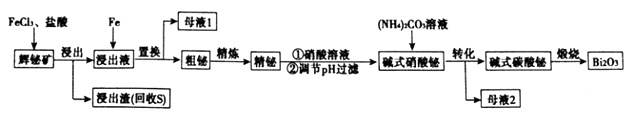
①“浸出”时Bi2S3与FeCl3 溶液反应的离子方程式为。
②“置换”时生成单质铋的离子方程式为。
③“粗秘”中含有的杂质主要是Pb,通过熔融盐电解精炼可达到除杂的目的,其装置示意图如所示。电解后阳极底部留下的为精铋。写出阳极电极反应的方程式。

试题篮