题型:实验探究题 题类:常考题 难易度:普通
浙江省宁波市宁波七中教育集团2022-2023学年九年级上学期科学期中学习效果自我评估试卷
【查阅资料】钠常温下就能与水发生剧烈反应,反应的化学方程式为2Na+2H2O=2NaOH+H2↑。
【提出猜想】猜想一:金属钠和硫酸铜溶液反应会有铜生成。
猜想二:金属钠和硫酸铜溶液反应,生成的沉淀只有氢氧化铜。
【实验及现象】切取不同大小的钠块分别投入到两种不同浓度的硫酸铜溶液中,有关产生沉淀的现象如表中所示。
|
实验编号 |
钠块大小 |
硫酸铜溶液 |
实验中产生沉淀的现象 |
|
① |
绿豆大小 |
稀溶液10mL |
产生蓝绿色沉淀 |
|
② |
绿豆大小 |
浓溶液10mL |
产生蓝色絮状沉淀 |
|
③ |
豌豆大小 |
稀溶液10mL |
产生蓝色絮状沉淀 |
|
④ |
豌豆大小 |
浓溶液10mL |
产生蓝色絮状沉淀,并出现黑色固体 |
小科咨询老师后得知蓝绿色沉淀为碱式铜盐。
【实验结论】
【实验反思】实验中生成氢氧化铜沉淀的原理是(用化学方程式表示)。
|
实验 序号 |
摆长(绳长)/厘米 |
摆动幅度/厘米 |
小球往返摆动20次的时间/秒 |
小球往返摆动1次的时间/秒 |
|
1 |
100 |
5 |
40 |
2.0 |
|
2 |
100 |
8 |
40 |
? |
|
3 |
80 |
5 |
30 |
1.5 |
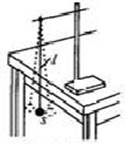
根据以上资料和实验数据,回答以下问题:
| 实验人 | 实验方案 |
| 小敏 | 第一天手背涂上防晒霜,第二天不涂。比较这二天被灼伤的程度。 |
| 小英 | 一只手背上涂上防晒霜,另一只手不涂。一天后,比较两只手背的灼伤程度。 |
| 小玲 | 在同学的手背上涂上防晒霜,自己不涂。一天后,比较自己手背与同穴手背被灼伤的程度。 |
| 小红 | 手心上涂上防晒霜,手背上不涂。一天后,比较手心与手背被灼伤的程度。 |
你认为最为合理的实验方案是( )
试题篮