题型:综合题 题类:模拟题 难易度:普通
贵州省贵阳市2021年高考理综-化学一模试卷
二甲醚(CH3OCH3)被誉为“21世纪的清洁燃料,由CO2和H2制备二甲醚的反应原理如下:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H1=-49.8 kJ•mol-1
反应II:CH3OCH3(g)+H2O(g) 2CH3OH(g) ∆H2= +23.4 kJ•mol-1
反应III:2CO2(g)+ 6H2(g) CH3OCH3(g)+3H2O(g) ∆H3
a.容器内混合气体的密度保持不变 b.消耗3molH2的同时生成1 mol H2O
c.反应体系总压强保持不变 d. CH3OH和CO2的物质的量之比保持不变
CH3OCH3(g) CH4(g)+ H2(g)+CO(g),在不同时间测定容器内的总压,所得数据见下表:
| 反应时间t/min | 0 | 5 | 10 | 15 | 20 | ∞ |
| 气体总压p总/kPa | 10.0 | 13.6 | 15.8 | 17.7 | 18.9 | 20.0 |
由表中数据计算:反应达平衡时,二甲醚的分解率为,该温度下的平衡常数Kp= (kPa)2. (Kp为用气体平衡分压代替气体平衡浓度表示的平衡常数,分压=总压×气体的物质的量分数)
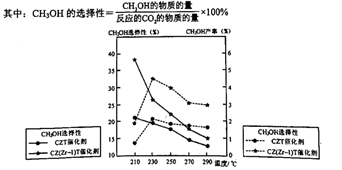
①温度高于230℃,CH3OH产率随温度升高而下降的原因是。
②在上述条件下合成甲醇的工业条件是。
a.230℃催化剂CZT b.210℃催化剂CZT
c.230℃催化剂 CZ(Zr-1)T d. 210℃催化剂CZ(Zr-1)T
I.过氧化氢是一种重要的物质,在科学研究和生产生活中应用广泛。
利用H2O2和KbrO3反应研究瞬时反应速率(r),原理为在酸催化下,KBrO3+3H2O2=KBr+3O2↑+3H2O。资料显示:r=k·cx(KbrO3)·cy(H2O2),其中k为速率常数。在290K测得实验数据如下:
实验编号 | 1 | 2 | 3 | 4 |
c(H2O2)/(mol/L) | 1 | 1 | 2 | 4 |
c(KBrO3)/(mol/L) | 0.003 | 0.006 | 0.001 | 0.001 |
R/(mol·L-1·s-1) | 3×10-4 | 6×10-4 | 8×10-4 | 6.4×10-3 |
试题篮