题型:综合题 题类:模拟题 难易度:普通
江苏省南通市2020年高考化学二模试卷
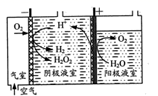
阴极表面发生的电极反应有:
Ⅰ.2H++O2+2e-=H2O2
Ⅱ. H2O2+2H++ 2e-=2H2O
Ⅲ. 2H+ +2e-=H2↑
①写出阳极表面的电极反应式:。
②其他条件相同时,不同初始pH(均小于2)条件下,H2O2浓度随电解时间的变化如图所示,c(H+)过大或过小均不利于H2O2制取,原因是。

H2O2(aq)+Mn2+(aq)=·OH(aq)+Mn3+(aq)+OH-(aq) ∆H=akJ/mol
H2O2(aq)+ Mn3+(aq) +2OH-(aq)= Mn2+(aq) +·O2-(aq) +2H2O(l) ∆H=bkJ/mol
·OH(aq) +·O2-(aq)=O2(g) +OH-(aq) ∆H=ckJ/mol
2H2O2(aq)= 2H2O(l)+O2(g) △H= 。该反应的催化剂为 。
①弱碱性条件下·OH将H2PO2-氧化成PO43- , 理论上l.7g·OH可处理含0.001mol/L H2PO2-的模拟废水的体积为。
②为比较不同投料方式下含H2PO2-模拟废水的处理效果,向两份等体积废水样品中加入等量H2O2和O3 , 其中一份再加入FeSO4。反应相同时间,实验结果如图所示:

添加FeSO4后,次磷酸盐氧化率、磷元素沉淀率均显著提高,原因是。
试题篮