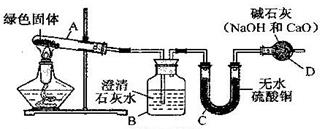
水煤气是一种工业上常用的气体燃料,一般用焦炭和水蒸气在高温下反应制得,含有少量的CO2和水蒸气杂质。某化学兴趣小组对水煤气的主要成分进行研究。
【查阅资料】
⑴白色的无水硫酸铜粉末遇水变成蓝色。
⑵Na2CO3与少量盐酸反应生成NaHCO3和NaCl,与过量盐酸反应时生成NaCl、H2O、CO2。
【实验假设】①可燃气体只是CO ②可燃气体只是H2 ③可燃气体是CO、H2的混合气。
【实验过程】实验小组按以下流程进行实验

实验中,发现黑色氧化铜变红,且无水硫酸铜变蓝色,还观察到澄清石灰水变浑浊,证明水煤气为{#blank#}1{#/blank#}(填实验假设的序号),根据实验现象写出无水硫酸铜的一种用途{#blank#}2{#/blank#}。
【实验反思】
根据实验结论,甲同学认为实验应保证安全,防止中毒,对尾气的处理方法是{#blank#}3{#/blank#}。
【实验拓展】实验后,乙同学认为欲检验所用NaOH是否完全消耗,可向溶液中滴入几滴稀盐酸,若没有气体产生,则溶液中还有NaOH剩余,但丙同学认为乙同学的设计是错误的,理由是(结合化学方程式解释){#blank#}4{#/blank#}。