修改时间:2024-07-13 浏览次数:289 类型:高考模拟
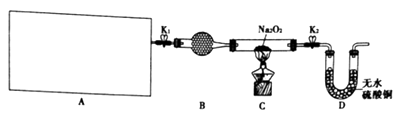
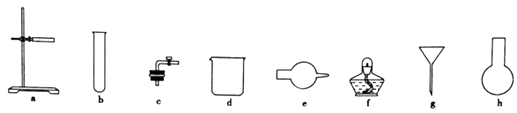
图中A是制取氢气的装置,从图所示的仪器中选择一部分组装成一套能随开随停的装置,选择的仪器编号是。
实验结束后,该同学欲测定C 装置硬质玻璃管内白色固体中未反应完的Na2O2含量。其操作流程如下: ![]()
①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和,操作2的名称是。
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数(填“偏 大” “偏小”或“不变”)。
C10H18(l) C10H12(l)+3H2(g) △H1
C10H12(l) C10H8(l)+2H2(g) △H2
△H1>△H2>0;C10H18→C10H12的活化能为Ea1 , C10H12→C10H8的活化能为Ea2 , 十氢奈的常压沸点为192℃;在192℃,液态十氢奈的脱氢反应的平衡转化率约为9%。请回答:
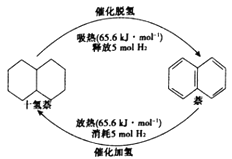
①在相同压强下升高温度,未达新平衡前,v正v逆(填写“大于”“小于”或“等于”)。
②研究表明,将适量的十氢奈置于恒容密闭反应器中,既升高温度又增大压强,十氢萘的转化率也升高,可能理由是。
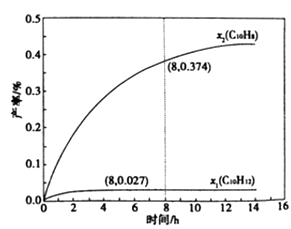
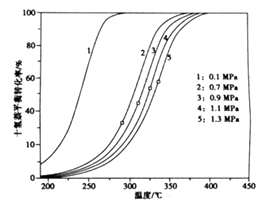
①在8h时,反应体系内氢气的量为mol(忽略其他副反应),液态十氢奈的转化率是。
②x1显著低于x2的原因是。
a.含氧酸的酸性:HNO3>H3PO4>H3AsO4
b.原子半径:S >P>As
c.氢化物的稳定性NH3>PH3> AsH3
d.AsH3电子式是 ![]()
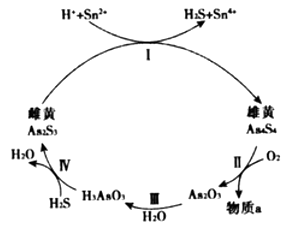
①Ⅱ中若1molAs4S4反应转移28mole- , a物质是。
②Ⅰ中反应的离子方程式是。

①人体血液的pH在7.35~7.45 之间,用药后人体中含砷元素的主要微粒是。
②H3AsO3的一级电离常数是6×10-10mol·L-1 , n(H3AsO3)∶n(H2AsO3-)=1∶1时,溶液的pH=(列出计算式即可)。
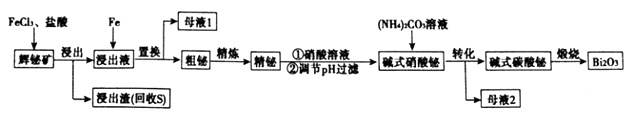
①“浸出”时Bi2S3与FeCl3 溶液反应的离子方程式为。
②“置换”时生成单质铋的离子方程式为。
③“粗秘”中含有的杂质主要是Pb,通过熔融盐电解精炼可达到除杂的目的,其装置示意图如所示。电解后阳极底部留下的为精铋。写出阳极电极反应的方程式。

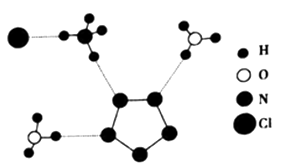
①图中R中阳离子是(填写化学式),相对分子质量较大的阳离子中心原子的杂化类型是。
②图中R中阴离子N5-中的σ键总数为个。分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
),则N5- 中的大π键应表示为。
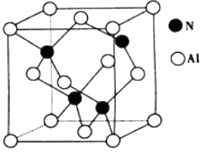
①已知氮化硼与X晶体类型相同,推测氮化硼的熔点比X的熔点(填“高”、“低“ ) ,可能的原因是。
②若X的密度为ρg·cm-3 , 则晶体中最近的两个Al原子的距离为cm。(阿伏加德罗常数的值用NA表示)
试题篮