题型:实验探究题 题类:模拟题 难易度:普通
上海市长宁区2017-2018学年中考化学二模考试试卷

请回答下列问题:
①甲中观察到的现象是 ,反应的化学方程式为 ; 乙中反应的现象是 ;
丙中反应的化学方程式为;丁中溶液由无色变成红色。
②当甲、乙试管内的固体完全溶解后,将两试管内的物质混合并加入过量的锌片、过滤,则滤渣的成分 是,滤液中溶质的化学式为。
③请设计能说明 NaOH 与H2SO4是否恰好中和的实验方案。(本题中所用过的试剂不能再用)
实验步骤 | 实验现象 | 实验结论 | |
④实验结束后,将乙(其中固体全部溶解)、丁两个实验的废液倒入同一个干净的废液缸中,静置,最终看到上层清液呈红色,废液下层有沉淀。由此推断上层清液的成分有酚酞、水和。 写出生成下层沉淀物的化学方程式。
通过上述实验可知,进行化学实验研究,除需要考虑生成什么物质外,还需要考虑。
选项 | 物质(括号内为杂质) | 除去杂质的方法 |
A | NaOH溶液 (Na2CO3) | 加入适量的Ca(OH)2溶液、过滤 |
B | CaO(CaCO3) | 加水溶解、过滤 |
C | CO(CO2) | 通过足量的NaOH溶液、干燥 |
D | FeSO4溶液(H2SO4) | 加入足量Fe粉、过滤 |
H2C2O4•2H2O 3H2O+CO↑+CO2↑
草酸晶体的其他性质如下:
熔点 | 沸点 | 溶解度(0℃) | 热稳定性 | 与碱反应 |
101℃~102℃ | 150℃~160℃ | 3.54g | 100.1℃失去结晶水,175℃分解成CO2 , CO,H2O | 与Ca(OH)2反应产生白色沉淀(CaC2O4) |
该小组设计的装置如下:图1是加热分解装置,图2是验证分解产物的装置.
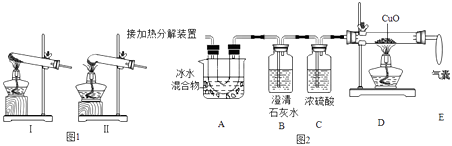
该小组称量纯碱草酸晶体的质量为10.0g,完全反应后A装置增加的质量为ag,B装置增加的质量为bg,D装置减少的质量为dg.实验过程中还能够观察到A中有液体和晶体.
试管编号 | 试管甲 | 试管乙 | 试管丙 |
所用试剂 | 稀盐酸 | 稀硫酸 | 稀盐酸 |
镁条 | 碳酸钠 | 氢氧化钡溶液 |

①混合前试管甲中盐酸一定剩余②混合前试管乙中稀硫酸一定剩余
③混合前试管丙中Ba(OH)2一定剩余④b→c时溶液的碱性逐渐增强
⑤c点处溶液中的离子只有Na+、Mg2+和Cl- ⑥反应前镁条的质量为
试题篮