题型:实验探究题 题类: 难易度:困难
吉林省长春市第一零三中学校2024-2025学年九年级上学期期中测试化学试题
某校学习小组的同学们准备测定某石灰石样品中碳酸钙的质量分数。
【提出问题】如何测定石灰石样品中碳酸钙的质量分数?
【实验设计】将样品与稀盐酸反应,测定反应后生成的体积,再根据体积换算为质量,最后根据
的质量求出样品中碳酸钙的质量。如图1为大理石与稀盐酸反应的反应装置,图2用于测量
的体积。

(1)图1检查装置气密性的操作是:。
(2)图1中,长颈漏斗的下端必须伸入液面以下这样做的目的是为便于获得平稳的气流,可用代替长颈漏斗。
(3)图2装置中油层的作用是。
(4)(填操作)可使反应前后油层上方气体压强和外界大气压相同,此时排出水的体积即为生成二氧化碳的体积。
【实验拓展】为进一步探究固体状态与产生气体的关系,同学们进行了实验:将采集到的样品用水冲洗后晾干,称取20.00g样品平均分成两份,分别与足量相同质量分数的稀盐酸反应进行下列测定(如图3),经数据处理得到释放出二氧化碳的质量与反应时间的关系图(如图4)。
(5)图3所示实验中数据记录纸上应该连续记录的实验数据是计时器读数和。

(6)由图4中曲线可以看出,固体物质与液体物质反应,当其他条件相同时,其影响实验的原因是。
(7)样品中碳酸钙的质量分数为。
【反思与评价】
(8)有同学认为图3装置不能准确测定产生的气体的质量,原因是。
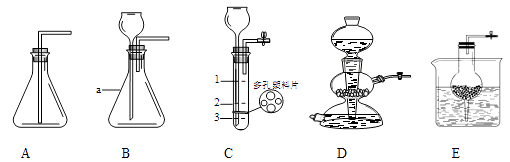
①写出仪器名称:a{#blank#}1{#/blank#},D的装置的名称是{#blank#}2{#/blank#}。此时D装置的开关处于{#blank#}3{#/blank#}状态(选填“开”或“关”)。E与D装置制取气体具有相同的优点是{#blank#}4{#/blank#}。
②观察A~E装置,{#blank#}5{#/blank#}装置(选填编号)进行实验时,集气瓶中不能收集得到二氧化碳,原因是{#blank#}6{#/blank#}。
③用C装置制取CO2 , 反应时装置内盐酸液面应位于{#blank#}7{#/blank#}处(选填“1、2或3”)为宜,理由是{#blank#}8{#/blank#}。
④测定其大理石中碳酸钙的质量分数。在15g大理石中分5次共加入50.0g稀盐酸(假设杂质不与盐酸反应,忽略盐酸的挥发),部分数据如下表。
容器中盐酸的质量 | 10 | 20 | 40 | 50 |
气体质量m/g | 1.1 | 2.2 | m | 4.4 |
根据实验数据回答下列问题:
Ⅰ. 当盐酸滴入40g时,对应的气体质量m是{#blank#}9{#/blank#}g。
Ⅱ. 大理石中碳酸钙的质量分数是{#blank#}10{#/blank#}。(根据化学方程式列式计算,结果精确到0.1%)
|
次数 |
1 |
2 |
3 |
4 |
|
加入稀硫酸质量/g |
70 |
70 |
70 |
70 |
|
剩余固体质量/g |
18.2 |
16.4 |
14.6 |
13.2 |
请计算:
(提出问题)所得溶液中所含溶质成分是什么?
(查阅资料)碳酸氢钠溶液呈碱性。
(提出猜想)猜想一:溶质为Na2CO3;
猜想二:溶质为NaHCO3;
猜想三:溶质为{#blank#}1{#/blank#}。
(设计实验)
|
实验步骤 |
实验现象 |
实验结论 |
|
①取所得溶液少许于试管中, 向其中滴加过量的CaCl2溶液; |
有白色沉淀生成 |
猜想二{#blank#}2{#/blank#}(填“成立”或“不成立”) |
|
②取实验步骤①中上层清液,滴加适量稀盐酸。 |
有气泡冒出 |
猜想一不成立 |
(得出结论)猜想三成立,证明二氧化碳通入碳酸钠溶液生成了碳酸氢钠。写出实验步骤②中发生反应的化学方程式:{#blank#}3{#/blank#};
(讨论交流)碳酸氢钠的俗名叫{#blank#}4{#/blank#}。小明同学认为,向碳酸钠溶液中通入一定量二氧化碳后,再向所得溶液中滴加几滴酚酞溶液,溶液变红就能证明一定有碳酸氢钠生成。小红同学对小明同学的结论产生质疑,其理由是{#blank#}5{#/blank#};
(拓展应用)同学们回忆在实验室用澄清石灰水检验二氧化碳的情景,结合上述知识,如果向一定量的澄清石灰水中不断通入二氧化碳气体,下列哪一个图像能符合题意反映生成的碳酸钙沉淀与二氧化碳的质量之间的变化关系{#blank#}6{#/blank#}(填字母)。

试题篮