水是宝贵的自然资料,让我们一起走进“水”的世界。
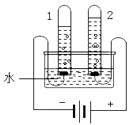
①下图电解水实验中,反应的化学方程式是{#blank#}1{#/blank#}。水电解过程发生改变的微粒名称是{#blank#}2{#/blank#}。
②医疗上常用0.9%NaCl溶液作生理盐水,配制1000g生理盐水需要氯化钠固体的质量为{#blank#}3{#/blank#}还可以制取碳酸饮料,该过程中发生反应的化学方程式为{#blank#}4{#/blank#}。
③某化学兴趣小组欲进行粗盐的初步提纯。粗盐的提纯实验步骤包括:a计算产率,b过滤,c溶解,d蒸发,e称量。实验步骤的正确顺序是:e、{#blank#}5{#/blank#}、a(填序号)。若NaCl的产率偏低,则可能的原因是{#blank#}6{#/blank#}(填字母)。
A.过滤时滤纸有破损 B.蒸发后所得精盐未完全蒸干,含有水
C.溶解含泥沙的粗食盐时,加入的水量不足
提示:产率=  ×100%
×100%
④已知KCl的溶解度20℃时为34g/100g水,40℃时为40g/100g水。某实验小组做了如下实验。

A中所得溶液中溶质与溶剂的质量比为{#blank#}7{#/blank#};溶质的质量分数相等的是{#blank#}8{#/blank#}。
I. B和C II. B和E III. C和D IV. D和E
