修改时间:2021-05-20 浏览次数:160 类型:开学考试
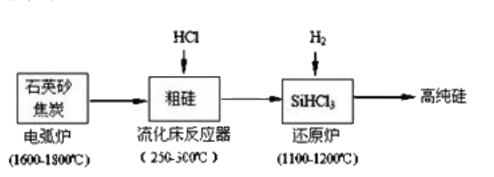
SiHCl3极易水解且生成某种可燃性气体,其完全水解的产物为_。
|
物质 |
Si |
SiCl4 |
SiHCl3 |
SiH2Cl2 |
SiH3Cl |
HCl |
SiH4 |
|
熔点/℃ |
1410 |
-70.4 |
-126.5 |
-122 |
-118 |
-114.2 |
-185 |
|
沸点/℃ |
2355 |
57.6 |
31.8 |
8.2 |
-30.4 |
-84.9 |
-111.9 |
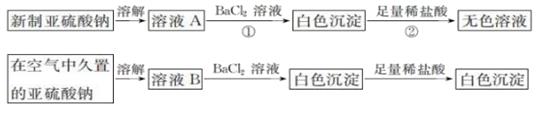
写出上述实验中②的离子方程式:。
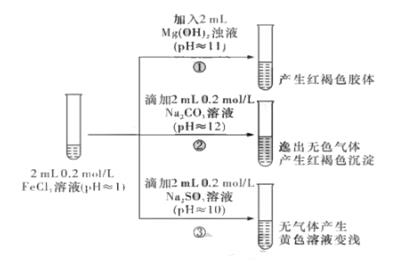
①中反应的离子方程式是._。
甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液, 产生白色沉淀。得出结论:
FeCl3与Na2SO3 发生了氧化还原反应,离子方程式是_。
乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是_。

①A中所用的试剂为。
②实验室用Na2SO3和硫酸制备SO2 , 可选用的气体发生装置是(选填编号)。

③B处反应管内五球中玻璃棉上的活性炭的作用为催化剂,D处U形管中盛放的试剂为其作用是:。

①钛的配位数为,原 子的杂化类型。
②该配合物中存在的化学键有 ( 填字母代号)。
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
|
TiCl4 |
TiBr4 |
TiI4 |
|
|
熔点/℃ |
-24.1 |
38.3 |
155 |
|
沸点/℃ |
136. 5 |
233. 5 |
377 |
分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是。


试题篮