题型:实验探究题 题类:模拟题 难易度:普通
江苏省南通市2017-2018学年高考理综-化学三模考试试卷
①根据生成气体的体积计算得到摩尔盐的纯度小于实际值,其原因是。
②向所得Fe(OH)2沉淀中加入NaNO2溶液可制得纳米Fe3O4 , 同时产生NO。该反应的离子方程式为。
①已知25 ℃,H2C2O4的电离常数Ka1=5.6×10-2 , Ka2=5.4×10-5。pH=4的H2C2O4溶液中c(C2O ):c(HC2O
)=。
②为了确定草酸合铁酸钾的组成,准确称取4.910 g样品在氮气气氛下加热,固体样品的剩余质量随温度的变化如图所示。
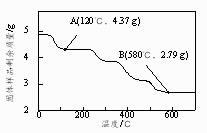
已知:a.120℃时已完全失去结晶水。
b.200℃~580℃分解产生的CO和CO2恢复至标准状况下体积为1.008 L。
c.580℃以上残留固体为FeO和K2CO3的混合物。
根据以上实验数据计算草酸合铁酸钾中的n(Fe3+):n(C2O42-)(写出计算过程)。
化学式 | 电离平衡常数(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |

部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
| 沉淀物 | Fe(OH) 3 | Fe(OH) 2 | Al(OH) 3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
请回答下列问题:
试题篮