题型:实验探究题 题类:常考题 难易度:普通
化学平衡的计算g 40
反应Ⅰ:CO(g)+2H2(g)⇌CH3OH(g)△H 1
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H 2
①表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K).
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断△H10 (填“>”、“=”或“<”).
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为,此时的温度为(从上表中选择).
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1=﹣1275.6kJ/mol
②2CO (g)+O2(g)=2CO2(g)△H2=﹣566.0kJ/mol
③H2O(g)=H2O(l)△H3=﹣44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
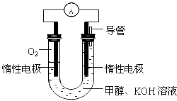
①该电池正极的电极反应为
②该电池总反应的离子方程式为
③工作一段时间后,测得溶液的pH(填“增大”、“减小”或“不变”).
试题篮