题型:实验探究题 题类:常考题 难易度:普通
河北省唐山遵化市2018-2019学年高二下学期化学期末考试试卷
甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是,由此可知分解产物中有(填化学式)。
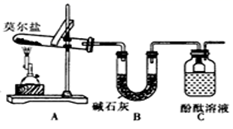
D. 品红溶液  E.NaOH溶液
E.NaOH溶液  F.BaCl2溶液和足量盐酸
F.BaCl2溶液和足量盐酸  G.排水集气法
G.排水集气法 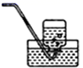 H. 安全瓶
H. 安全瓶 ![]()
①乙同学的实验中,装置依次连按的合理顺序为:A→H→() →() →() →G。
②证明含有SO3的实验现象是;安全瓶H的作用是。
甲方案:取25.00mL样品溶液用0.1000mol/L的酸性K2Cr2O7溶液分三次进行滴定。
乙方案(通过NH4+测定):实验设计装置如图所示。取25.00mL样品溶液进行该实验。
请回答:
甲方案中的离子方程式为。
a.水 b.饱和NaHCO3溶液 c.CCl4 d.饱和NaCl溶液
石蕊试液 | 品红溶液 | 饱和硫化氢溶液 | 氯水 | |
A | 无色 | 无色 | 乳白色浑浊 | 无色 |
B | 红色 | 无色 | 黄色浑浊 | 无色 |
C | 红色 | 无色 | 乳白色浑浊 | 黄绿色 |
D | 无色 | 无色 | 乳白色浑浊 | 黄绿色 |
试题篮