题型:实验探究题 题类:常考题 难易度:普通
江西省吉安市七校联盟2019-2020学年九年级上学期化学期中考试试卷

(猜想与假设)
①速率慢、气泡少可能与过氧化氢溶液的浓度有关。
②速率慢、气泡少可能与MnO2的质量有关。
(进行实验)根据右图进行如下实验。
实验1:用26mgMnO2与5mL不同浓度过氧化氢溶液进行实验,压强变化如图1。
实验2:用5mL1.5%过氧化氢溶液与不同质量MnO2进行实验,压强变化如图2。


(解释与结论)
小组同学在制取氧气过程中,发现反应的速率很慢,产生的气泡很少的原因可能是。
H2C2O4•2H2O 3H2O+CO↑+CO2↑
草酸晶体的其他性质如下:
熔点 | 沸点 | 溶解度(0℃) | 热稳定性 | 与碱反应 |
101℃~102℃ | 150℃~160℃ | 3.54g | 100.1℃失去结晶水,175℃分解成CO2 , CO,H2O | 与Ca(OH)2反应产生白色沉淀(CaC2O4) |
该小组设计的装置如下:图1是加热分解装置,图2是验证分解产物的装置.
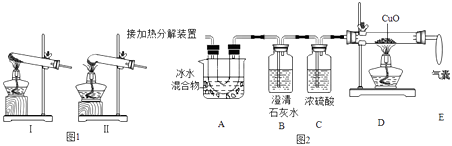
该小组称量纯碱草酸晶体的质量为10.0g,完全反应后A装置增加的质量为ag,B装置增加的质量为bg,D装置减少的质量为dg.实验过程中还能够观察到A中有液体和晶体.
【问题】氧化铝能不能做过氧化氢分解的催化剂?
【猜想】氧化铝能做过氧化氢分解的催化剂
【实验验证】
实验步骤 | 实验现象 | 实验结论 | |
实验一 | {#blank#}1{#/blank#} | 木条不复燃 | 常温下过氧化氢溶液不分解 |
实验二 | 在装有过氧化氢溶液的试管中加入少量氧化铝,然后将带火星的木条伸入试管中 | 木条复燃 | {#blank#}2{#/blank#} |
【结论】氧化铝能加快过氧化氢的分解速率,故氧化铝能做过氧化氢分解的催化剂
【讨论与反思】经过讨论,有的同学认为只有上述两个证据,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:【实验目的】探究{#blank#}3{#/blank#}.
【实验步骤】①准确称量氧化铝(少量)的质量;②完成实验二③待反应结束,将实验而试管里的物质进行过滤,洗涤,{#blank#}4{#/blank#},{#blank#}5{#/blank#};对比反应前后氧化铝的质量。
【讨论】如果氧化铝在反应前后质量不变,则说明氧化铝可以做过氧化氢分解的催化剂。
但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验{#blank#}6{#/blank#}.请简述操作和现象:①{#blank#}7{#/blank#}.②{#blank#}8{#/blank#}。
试题篮