修改时间:2021-12-01 浏览次数:110 类型:二轮复习


| 编号 | 稀硫酸(%) | NaOH溶液(%) | 温度变化/℃ |
| 1 | 9.8 | 4.0 | 3.8 |
| 2 | 9.8 | 8.0 | 7.6 |
| 3 | 9.8 | 12.0 | 7.6 |
| 4 | 19.6 | 16.0 | 15.2 |
反应的方程式为: 2NaOH+H2SO4=Na2SO4+2H2O
|
实验组别 |
一 |
二 |
三 |
四 |
|
稀盐酸质量/克 |
100.0 |
100.0 |
100.0 |
100.0 |
|
混合物质量/克 |
3.0 |
6.0 |
9.0 |
12.0 |
|
所得溶液质量/克 |
101.9 |
103.8 |
105.0 |
a |
|
剩余固体质量/克 |
0 |
0 |
>0 |
>0 |
已知氯化钙溶液为中性,请回答:
|
实验组别 |
一 |
二 |
三 |
|
稀盐酸质量(g) |
100. 0 |
100. 0 |
100. 0 |
|
混合物质量(g) |
3.0 |
6.0 |
9.0 |
|
所得溶液质量(g) |
101. 9 |
103. 8 |
105. 0 |
|
剩余固体质量(g) |
0 |
0 |
a |
求混合物中氯化钙的质量分数(要求写出计算过程,结果保留1位小数)。

小明同学是一次性先收集7瓶不同氧气体积分数的气体,然后逐一检验是否能使带火星的木条复燃。实验结果记录,如表甲。
|
第1瓶 |
第2瓶 |
第3瓶 |
第4瓶 |
第5瓶 |
第6瓶 |
第7瓶 |
|
|
氧气含量 |
30% |
40% |
50% |
60% |
70% |
80% |
90% |
|
带火星木条 |
不复燃 |
复燃 |
复燃 |
复燃 |
复燃 |
复燃 |
复燃 |
小王同学是先收集一瓶气体,检验它能否使带火星的木条,分析后再依次收集下一瓶气体再进行实验。实验结果记录,如表乙:
|
第1瓶 |
第2瓶 |
第3瓶 |
第4瓶 |
第5瓶 |
|
|
氧气含量 |
60% |
40% |
30% |
35% |
32.5% |
根据实验结果,你认为哪位同学的方法更好?并说出你的依据。。

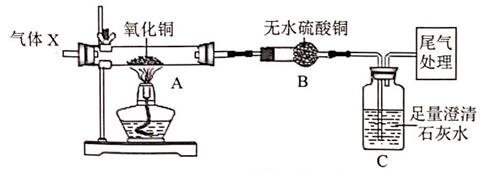
①气体X与氧化铜反应处生成铜外还可能生成氧化亚铜(Cu2O);
②铜和氧化亚铜均为不溶于水的红色固体,
③Cu2O + H2SO4=CuSO 4+ Cu +H2O。
小乐为了探究反应所得红色固体的成分,进行了如下实验:
|
实验操作 |
实验现象 |
实验结论 |
|
|
步骤一 |
取20g红色固体于烧杯中,加入足量稀硫酸 |
|
红色固体可能是氧化亚铜也可能是铜和氧化亚铜 |
|
步骤二 |
将步骤一反应所得的混合物经过滤、洗涤、干燥并称量剩余红色固体质量 |
剩余红色固体质量为12g |
20g红色固体中,铜和氧化亚铜的质量比为。 |

请回答:
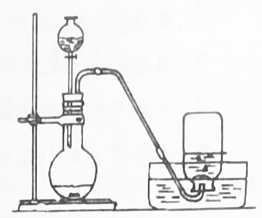
[查阅资料]①浓硫酸既可吸收水,也可吸收氨气
②NH3+HCl=NH4Cl
③2NH3+3CuO 3Cu+N2+3H2O

[实验分析]
B装置是利用了浓硫酸具有性。
[实验结果]原混合气体中各物质的组成情况是。(算出质量)
试题篮