修改时间:2024-07-13 浏览次数:251 类型:期末考试
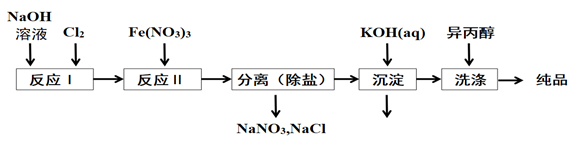
①洗涤粗品时选用异丙醇而不用水的理由是:。
②反应II的离子方程式为。
③高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为它能净水的原因是。
中加入饱和KOH溶液,即可析出高铁酸钾。
①加入饱和KOH溶液的目的是:。
②由以上信息可知:高铁酸钾的溶解度比高铁酸钠(填“大”或“小”)。
|
湿法 |
强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
|
干法 |
Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
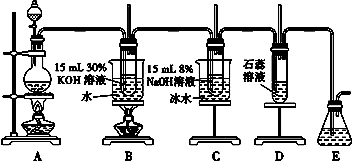
写出装置A实验室制取Cl2的化学方程式。
实验小组利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中CO2的影响)。
①提出合理假设
假设1:只存在SO32-;假设2:既不存在SO32- , 也不存在ClO-;假设3:。
②设计实验方案,进行实验。请完成下列表格,写出相应的实验步骤以及预期现象和结论。
限选实验试剂:3 mol· L-1 H2SO4、1 mol· L-1NaOH溶液、0.01 mol· L-1酸性KMnO4溶液、淀粉KI溶液。
|
实验步骤 |
预期现象和结论 |
|
步骤1:取少量吸收液分置于A、B试管中 |
|
|
步骤2:向A试管中滴加0.01 mol·L-1酸性KMnO4溶液 |
若溶液褪色,则假设1成 |
|
若溶液不褪色,则假设2或3成立 |
|
|
步骤3: |
|

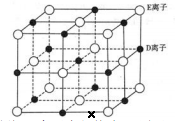
若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示 A的一种晶体的晶胞(已知 A—A 键的键长为a cm, NA表示阿伏加德罗常数),则该晶胞中含有个 A 原子,该晶体的密度是g·cm-3(列式表示) 。

已知:两个醛分子在NaOH溶液作用下可以发生反应,生成一种羟基醛:
![]() +
+ ![]()
![]()
![]()
请回答:
反应④的化学方程式:。
![]()
试题篮