修改时间:2024-07-12 浏览次数:1288 类型:中考模拟
②在化学变化中,物质的转化遵循质量守恒定律.一定质量的某物质甲(相对分子质量是90)在氧气中完全燃烧,消耗6.4g氧气,同时生成5.6g一氧化碳、4.4g二氧化碳和5.4g水,则对甲的说法正确的是(填字母序号).
A.只含有碳、氢两种元素
B.一定含有碳、氢元素,可能含有氧元素
C.碳元素质量分数为40%
D.若相同质量的甲在9.6g氧气中完全燃烧,则只生成二氧化碳和水.
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
某兴趣小组做了以下实验:

步骤I:将⑤继续冷却至0℃,过滤,共可回收得到KNO3固体 g.
步骤II:向滤液中加入 g水稀释,得到溶质的质量分数为1%的KNO3稀溶液,将此溶液做为花肥使用.

【资料】Fe+2FeCl3=3FeCl2
①Ⅱ中反应的化学方程式是.Ⅲ中反应的化学方程式是.
②结合上述流程,下列说法不正确的是(填序号).
a.反应Ⅰ的化学方程式为:4FeS2+11O2 2Fe2O3+8SO2
b.上述流程所涉及的物质中,硫元素的化合价有﹣2.+4.+6
c.若向溶液乙和丙的稀溶液中分别加入足量的甲,会观察到完全相同的现象
d.假设转化过程中无损失,150t含FeS280%的硫铁矿最多可以制得98t硫酸.

已知SO2能使红色的品红溶液褪色,也能使澄清石灰水变浑浊,而CO2不能使红色的品红溶液褪色;SO2能被酸性高锰酸钾溶液吸收而除去,而CO2不能被酸性高锰酸钾溶液吸收.
试用下图所列各种装置设计一套实验来验证浓硫酸与木炭反应所得到的各种产物.这些装置的连接顺序(按产物气流从左到右的方法)是→→ → (填写装置的编号).

则A瓶的作用是;
B瓶的作用是;
C瓶的作用是.
①CuSO4溶液与NaOH溶液、②CuSO4溶液与BaCl2溶液反应.实验结束后将两次实验中的废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色.
【提出问题】滤液中溶质的成分是什么?
【作出猜想】小红认为:只含氯化钠;
小明认为:可能含有硫酸钠、氯化钠和氯化钡;
小亮认为:可能含氯化钠和氯化钡;
你认为:还可能是(写一种猜想).
【讨论】你认为小红、小明、小亮三位同学中谁的猜想明显不合理?为什么?
【实验探究】
实验操作 | 实验现象 | 实验结论 |
实验A:取少量滤液于试管中,加入 适量纯碱溶液,振荡. | 无明显现象 | 滤液中不含 |
实验B:取少量滤液于试管中,加入适量硝酸钡溶液,振荡. | 产生白色沉淀 | 滤液中含有 |
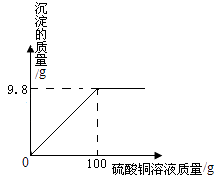
b.在盛有100g氢氧化钠溶液的大烧杯中缓缓加入硫酸铜溶液,反应生成沉淀的质量与加入硫酸铜溶液质量的关系如图所示:求恰好完全反应时,所得溶液中溶质的质量分数?(精确到0.1% )
试题篮