修改时间:2024-07-13 浏览次数:704 类型:期末考试
反应Ⅰ.Ca(ClO)2+2H2O=Ca(OH)2+2HClO
反应Ⅱ.2NaCN+2HClO+Ca(OH)2=2NaCNO +2H2O +CaCl2(CNO-中C为+4)
反应Ⅲ.NaCNO+HClO- +H2
+N2
+NaCl(未配平)
①反应Ⅱ中氧化剂是(写化学式),氧化产物与还原产物的物质的量之比
为。
②若反应Ⅲ中转移0.6mol电子,则生成的气体在标准状况下的总体积是


回答下列问题:
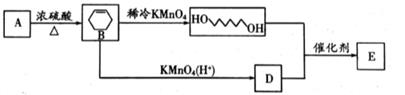
①A的化学名称为
②生成E的化学方程式为
个平面上的A的结构简式为分子中存在 ,且存在顺反异构体的A的反式异构体的结构简式为
中存在“-OH”、“ ![]() ”和两个“
”和两个“ ”,且分子中存在两个手性碳原子。则A的结构简式为

回答下列问题:


①B中溶液为
②A中装有蒸馏水,查阅资料可知次氯酸或氯气可被SO2 , H2O2 , FeCl2等物质还原成Cl- , 请设计实验方案测定A中氯元素含量

回答下列问题:
可选试剂:稀硫酸、稀盐酸、KSCN溶液、KMnO4溶液、NaOH溶液
试题篮