在常温下,向10 mL浓度均为0.1 mol·Lˉ
1的NaOH和Na
2CO
3混合溶液中滴加0.1 mol·Lˉ
1的盐酸,溶液pH随盐酸加入体积的变化如图所示。 下列说法正确的是( )
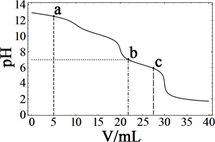
A、在a点的溶液中,c(Na+)>c(CO32-)>c(Clˉ)>c(OH‾)>c(H+)
B、在b点的溶液中,2n(CO32-)+n(HCO3-)<0.001 mol
C、在c点的溶液pH<7,是因为此时HCO的电离能力大于其水解能力
D、若将0.1 mol·Lˉ1的盐酸换成同浓度的醋酸,当滴至溶液的pH=7时:c(Na+)=c(CH3COOˉ)
