题型:实验探究题 题类:常考题 难易度:普通
化学平衡的计算g 40
FeO(s)+CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+ CO(g)═
Fe3O4(s)+
CO2(g)△H2
Fe3O4(s)+4CO(g)═3Fe(s)+4CO2(g)△H3
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H4
则△H4的表达式为(用含△H1、△H2、△H3的代数式表示).
温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600℃时固体物质的主要成分为,该温度下若测得固体混合物中.
m(Fe):m(O)=35:2,则FeO被CO还原为Fe的百分率为(设其它固体杂质中不含Fe、O元素).
t/min | 0 | 10 | 20 | 30 | 40 | 50 |
x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
①能判断CO(g)+3H2(g)⇌CH4(g)+H2O(g)达到平衡的是(填序号).
a.容器内压强不再发生变化
b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2)
d.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO的转化率为;
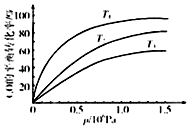
③图表示该反应CO的平衡转化率与温度、压强的关系.图中温度T1、T2、T3由高到低的顺序是,理由是.
试题篮