题型:综合题 题类:常考题 难易度:普通
晶体硅是一种重要的非金属材料,模拟制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HClSiHCl3+H2 ,
沸点/℃ | |
SiHCl3 | 33.0 |
SiCl4 | 57.6 |
HCl | ﹣84 |
③SiHCl3与过量H2在1000~1100℃反应制得纯硅可能用到的信息如下:
已知SiHCl3能与H2O强烈反应,在空气中易自燃;
步骤②中粗硅与HCl反应时会生成少量SiCl4;
请回答下列问题:
用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):

①依次连接的合理顺序为 ;装置D中g管的作用是 ;装置B中的试剂是 ;装置C中的烧瓶加热的目的是 .
②装置A中发生反应的化学方程式为 .
③操作时应先打开装置 (C或D)中分液漏斗的旋塞,理由是:
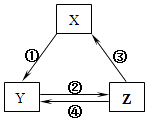
|
选项 |
X |
Y |
Z |
箭头上所标数字的反应条件 |
|
A |
SiO2 |
Na2SiO3 |
H2SiO3 |
①与Na2CO3熔融 |
|
B |
Na |
Na2O2 |
NaCl |
②加H2O |
|
C |
NO |
NO2 |
HNO3 |
③与C加热 |
|
D |
Al2O3 |
NaAlO2 |
Al(OH)3 |
④与NaOH |
试题篮