题型:单选题 题类:常考题 难易度:普通
2016年新人教版初中化学湖北省咸宁初三下册第12单元化学与生活练习卷
如下图是甲、乙两位同学一起在实验室进行的氢氧化钠与盐酸中和反应的实验。
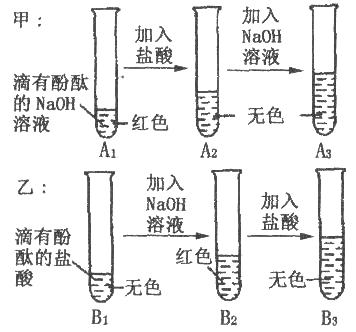
(说明:图中A1、A2、A3、B1、B2、B3均为溶液编号)
根据如图实验,请你与甲、乙同学一起完成下列探究:
探究环节 | 甲同学的探究 | 乙同学的探究 |
提出问题 | A3溶液为什么不变红? | B3溶液中溶质成分是什么?(酚酞不计) |
做出猜想 | 实验过程中,酚酞变质了? | 猜想一:NaCl 猜想二:NaCl HCl |
实验验证 | ①取少量A3 , 溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想{#blank#}1{#/blank#}(填“成立”或“不成立”); ②你认为,在常温下A2溶液测出的pH应{#blank#}2{#/blank#}(填“>”、“=”或“<”)7。 | 取少量B3溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变{#blank#}3{#/blank#},据此,你认为乙同学的猜想{#blank#}4{#/blank#}(填“一”或“二”)成立。 |
交流反思 | ①甲、乙同学的实验中,反应均涉及到的化学方程式是{#blank#}5{#/blank#}; ②A3溶液未变红,你认为原因是A2溶液中{#blank#}6{#/blank#}较多,加入的NaOH溶液未将其完全中和; ③甲、乙同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制。 | |
T⋅f菌(见图1)是一种细菌,用T⋅f菌脱除工业废气中的一种有毒、有腐蚀性的气体—硫化氢(H2S)。其作用原理如图2所示。用这种方法处理废气大大降低了治污的成本,脱除率达到99.97%,且无废物排出。但要达到高效的关键是要保证体系内FeSO4浓度的稳定,一旦FeSO4浓度降低,T⋅f菌就会像缺少食物一样逐渐失去活性。实际应用过程发现,Fe2(SO4)3在pH=1.9时会发生一定的变化,生成了铁的沉淀物—黄铵铁矾[NH4Fe3(SO4)2(OH)6],并在pH=3.2时沉淀完全,使得溶液中的总铁浓度下降,降低了对废气的吸收效率。

实验测得30℃时,不同pH环境下T⋅f菌的活性也不同。表现为FeSO4溶液转化为Fe2(SO4)3溶液的速率不同,如下表:
pH | 0.9 | 1.2 | 1.5 | 1.9 | 2.1 | 2.4 | 2.7 | 3.0 |
FeSO4溶液转化为Fe2(SO4)3速率/(g⋅L-1⋅h-1) | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 | 6.2 | 5.6 |
回答下列问题:
试题篮