题型:实验探究题 题类:常考题 难易度:普通
浙江省温州十校联合体2018-2019学年高一上学期化学期末考试试卷
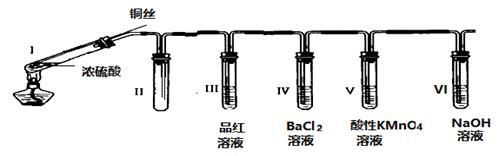
请回答:
A BaCl2溶液 B 铁粉 C NaHCO3溶液 D 银粉
| A | B | C | D | |
| 实验 | 分离植物油和氯化钠溶液 | 除去氯化钠晶体中混有的氯化钾晶体 | 分离CCl4中的Br2 | 除去CO2气体中的HCl气体 |
| 装置 或仪器 | | | | |
试题篮