题型:实验探究题 题类:常考题 难易度:普通
山西省长治市上党联盟2018-2019学年高一下学期化学期末考试试卷
①该反应为(填“放热”或“吸热”)反应,因此在该反应中,断裂化学键吸收的能(填“大于”或“小于”)形成化学键放出的能量。
②下列措施中,能加快氢气生成速率的是(填字母)。
a.将铁片改成铁粉
b.降低稀H2SO4的温度
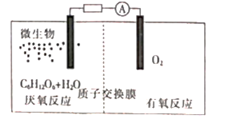
①有氧反应一极是电池的(填“正”或“负”)极,质子交换膜允许 通过,该电池的正极反应式为
②若该电路中转移电子的物质的量为12 mol,则生成CO2的体积(标准状况)为
|
| 图像 | 结论 |
| A | | 相同质量锌粉分别与 1mol/ L 盐酸及相同体积未知浓度的盐酸反应,未知浓度盐酸的浓度低于 1mol/ L |
| B | | 一定条件下,金刚石转化为石墨要释放能量,金刚石要比石墨稳定 |
| C | | 该装置为化学能转化为电能的装置,且 Mg 作负极 |
| D | | 试纸中心区域变黑,边缘变红,可知浓硫酸具有脱水性 |
试题篮