修改时间:2024-07-12 浏览次数:446 类型:月考试卷
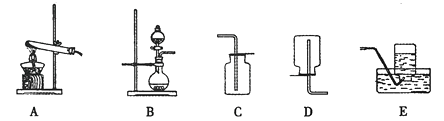
有约占总体积40%水,氧气从(填“a”或“b”)导管口进入,排尽集气瓶中的水,收集氧气后集气瓶中氧气的体积分数是。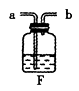
①称取12g样品放入烧杯;
②加入足量的稀盐酸至不再产生气体时,过滤、洗涤、干燥后称量剩余固体质量为3.6g;
③根据剩余固体的质量求出样品中碳酸钙的质量分数为。
①称取6g样品:按规范操作,用托盘天平称取6g样品时,若指针略向左偏转,要使指针居中的恰当操作是:;把称取好的样品放入烧杯中(烧杯质量为10g).
②将50g稀盐酸分5次加入,每次加入稀盐酸后,用玻璃棒不断搅拌,搅拌的目的是 ,然后对烧杯(包括溶液和残余固体)进行了称量,记录如下表:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的总质量(g) | 10 | 20 | 30 | 40 | 50 |
烧杯和药品总质量(g) | 25.56 | 35.12 | 44.68 | 54.24 | 64.24 |
①样品完全反应后生成二氧化碳的质量为g.
②石灰石样品中碳酸钙的质量分数是多少?(计算结果精确到0.1 %)
③最后所得溶液的质量为g.
试题篮