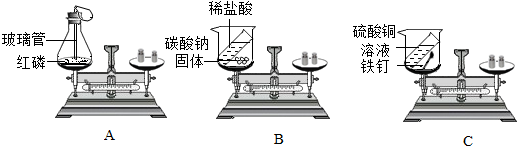
(1) 实验A中锥形瓶底部预先铺一层薄薄的细沙的目的
(2) 实验A中观察到锥形瓶内红磷燃烧的化学方程式:
(3) 实验A中观察到锥形瓶内红磷燃烧,气球现象是,装置放回天平后天平
(4) 上述三个反应前后容器中物质的总质量不相等的是,符合质量守恒定律的是(均填实验装置序号)
(5) 实验B中,最终天平不平衡的原因是碳酸钠和盐酸反应生成的气体逸散空气中,最终没有称量到所有生成物的总质量。
(6) 实验C观察到烧杯内色固体(铁钉)表面产生,溶液由色变成色,此反应的化学方程式为
(7) 由实验A,B,C可知要设计探究验质量守恒定律,实验的改进方法是。