修改时间:2024-07-13 浏览次数:153 类型:期末考试

已知:
①卤块的主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质
②四种化合物的溶解度(S)随温度(T)变化的曲线如图所示。
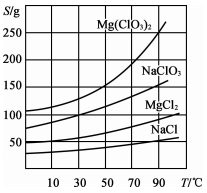
回答下列问题:
步骤1:准确称量3.50g产品配成100mL溶液。
步骤2:取出10.00mL溶液于锥形瓶中,加入10.00mL稀硫酸和21.00mL.1.000mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100mol·L-1K2Cr2O7溶液滴定剩余的Fe2+至终点[发生的反应为Cr2O72-+Fe2++H+→Cr3++Fe3++H2O(未配平)]
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00mL
步骤2中发生反应的离子方程式为。该样品中Mg(ClO3)2·6H2O的纯度为(保留两位有效数字)。
H2SeO3(aq)+2SO2(g)+H2O(l)=Se(s)+2H2 SO4(aq) △H1
2H2SeO4(aq)+Se(s)+ H2O (l)=3H2SeO3(ag) △H2
H2SeO4(aq)+ 3SO2(g)+2H2 O(l)=Se(s)+3H2 SO4 (aq) △H3
则△H2=(用△H1和△H3表示)。

①阳极的电极反应式为。
②电解一段时间后,向电解液中补充一定量的可将溶液恢复至初始状态。
CO(g)+2H2(g) CH3OH(g) △H=akJ·mol-1。
按 的投料比将H2与CO充人VL的恒容密闭容器中,在一定条件下发生反应,测定CO的平衡转化率与温度、压强的关系如图2所示。
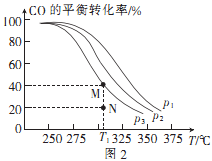
①a(填“>”或”<”)0;压强p1、p2、p 3由小到大的顺序是。
②T1℃时,若向该容器中充入2.0mol H2和2.0 mol CO发生上述反应,5min后反应达到平衡(M点),则0~5min内,v(H2)=mol·L-1·min-1 , N点对应条件下反应的平衡常数为。
a.氟化钙
b.金刚石
c.钠
d.氯化铯
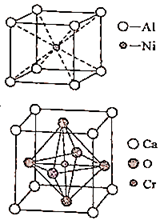
①该晶体的化学式为。
②已知钙离子、氧离子半径分别为100pm、140pm,该晶胞的参数(边长)为pm。
③阿伏加德罗常数的值为NA , 该晶体密度的计算表达式为g·cm-3;晶胞中Cr4+位于O2-所形成的正八面体的体心,该正八面体的边长为pm。
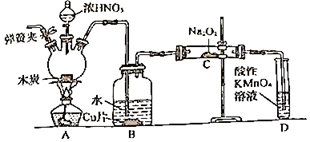
已知:
室温下,①2NO+Na2O2=2NaNO2
②3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O
③酸性条件下,NO或NO2ˉ都能与MnO4ˉ反应生成NO3ˉ和Mn2+
回答下列问题:

已知:①烃A是最简单的烯烃
②醛与醛能在一定条件下反应,原理如下:

回答下列问题:
①除苯环外不含有其他环状结构;②能发生水解反应和银镜反应。
其中核磁共振氢谱显示为5组峰,且峰面积比为1:1:2:2:2的是(写结构简式)
试题篮